私達の研究室では広範な領域の生命医科学研究を数理情報科学の観点からお手伝いさせていただいてまいりました。現状の我々に対応可能な「バイオインフォマティクス解析」「AI構築」「システム生物学・数理モデル解析」「コンピューター創薬」を平易にご紹介いたします。もしご興味のあるものがありましたら、遠慮なくメールを清水あてにお送りください。私は内科医としての臨床経験もありますし基礎的な分子生物学実験で博士号をとりました。このように臨床も生命科学実験も経験している情報科学のチームだからこそ、実験系/臨床の先生方と同じ共通言語でdiscussionできると自負しております。生命科学や医療の研究を精力的に進めていらっしゃる先生方との新たな出会いを心待ちにしております。
バイオインフォマティクス ・クリニカルインフォマティクス関連
バイオ (生命科学/基礎医学) とクリニカル (臨床医学) 領域の情報科学解析を行っています。共同研究としては、主に下記2点を担当させていただける可能性があります。
NGS /オミクスデータ解析
トランスクリプトーム・プロテオーム・メタボロームデータなどの解析です。マルチオミクスデータを統合するトランスオミクス解析も実施可能です。NGS解析受託企業が提供する一般的な遺伝子発現変動解析、エンリッチメント解析、多変量解析などに加えて、メカニズムに基づくマルチオミクスデータの統合 (トランスオミクス解析) も可能です。対象とする疾患もがん・感染症・生活習慣病のように広範な領域を扱ってきましたし、疾患とは関係なく純粋な生命科学研究にも携わってまいりました。私達が関わっている主要ジャーナルに掲載された解析例としては、Kodama et al. Cell Reports 2023 ; Ichihara et al. Nucleic Acids Research 2021; Kokaji et al., Science Signaling 2020; Aso et al., Cell Reports 2020 他多数あります。
いくつか具体的に列挙すれば、まずトランスクリプトーム解析 (Bulk RNA-seq、マイクロアレイ) については、クオリティコントロール (QC) からはじまりマッピング・遺伝子発現行列取得、発現変動遺伝子 (DEG) の抽出、Gene Ontology解析、スプライシングバリアントの検出、変異塩基の検出あたりが定番どころの解析です。
シングルセルRNA-seq (scRNA-seq) も細胞クラスタリング・アノテーション・RNA velocity解析といった一般的なものだけにとどまらず、テンソル分解を用いた条件特異的発現パターンの抽出、転写因子活性パターンの推定、細胞間相互作用の推定、TCR配列再構築によるレパトア解析等も手掛けております。
ChIP-seq/ATAC-seq, scATAC-seqについても、遺伝子制御ネットワーク解析を含むさまざまな解析に対応可です。
また、ゲノム解析についてはモデル動物・非モデル動物のみならず細菌やウイルスといった微生物についても遺伝子のゲノムマイニングや種間比較、トランスポゾン解析などをやってきております。
臨床統計データ解析
主に臨床データ・コホートの統計解析支援を行っています。傾向スコアや差の差の解析、やや発展的な生存時間解析、webサーバーからのデータの自動抽出、メタアナリシス等々をサポートしています。私達が関わっている主要ジャーナルに掲載された解析例としては、Habara et al. PNAS 2022 ; Kodama et al. Nature Communications 2020 ; Onoyama et al. Cancer Research 2020 ; Oshikawa et al. Oncogene 2020 ; Muto et al. Journal of Experimental Medicine 2019 他多数あります。
機械学習・AI関連
機械学習とは機械に人間の知能を模倣したような知的作業をコンピュータに行わせる「人工知能(AI)」に含まれる概念で、与えたデータに隠されたルールやパターンといった法則を発見させる手法です。更に、その発見した法則が原因と結果をを繋ぐものである場合は、それを利用して原因からその結果を予測できるため、多くの場合は予測を目的として学習が行われます。その機械学習の一部として近年大きく発展しているのが、深層学習です。画像認識AIや翻訳AI、またChatGPTのような生成AIなどがこれに含まれます。
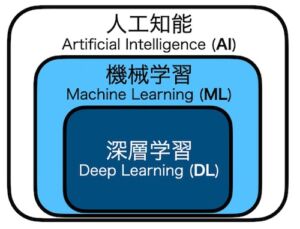
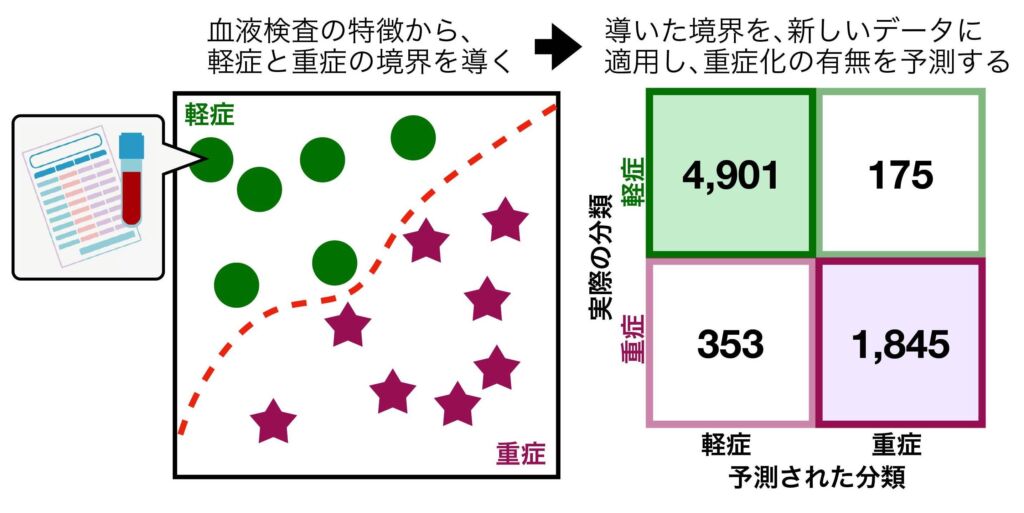
機械学習で行えることの1つは、分類問題を解く、簡単にいうと数字認識のようにデータを種類に分けることです。バイオ系だと、このタンパクAとBは結合するかしないかとか、このゲノム領域は翻訳される / されないだとか、医療データでは正常組織とがん組織の分類や入院時の検査データからの重症化の有無の予測、心電図の不整脈検出といった課題を解くことができます。
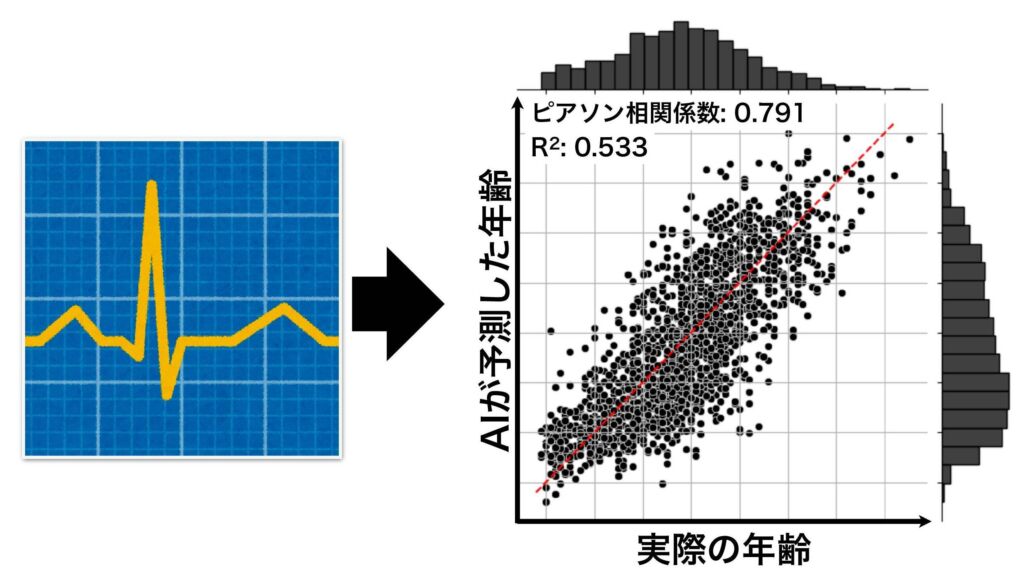
機械学習をもとに、データの特徴から何らかの数値を予測する回帰モデルを作ることもできます。例えば、心電図データから年齢や電解質の数値を予測したいといった用途にも対応できます。
他にも、例えばいろいろながんの遺伝子発現パターンの比較や、治療前後の検査データの比較など、人の目では判別が困難な類似度の評価にも機械学習は有用です。
分類問題・回帰問題に限らず、正解データがない場合には教師なし学習は半教師あり学習という手法もありますし、また近年隆盛を見せている生成AIにも対応できます。
エクセルのような表形式のデータはもちろん、機械学習は顕微鏡写真・レントゲンやCT/MRIといった画像データにもアフィニティーが高いです。それ以外に、医療を含む広い意味のありとあらゆるライフサイエンスデータに機械学習は使われるようになっており、我々も抗がん剤の探索、神経難病の基礎研究からハイスループットイメージング、より臨床に近いところでは手術前の臨床情報から長期予後を予測するモデルまでさまざまな機械学習に取り組んできました。私達が関わっている主要ジャーナルに掲載された解析例としては、Hozumi et al. PNAS Nexus 2023 ; Shimizu et al. iScience 2022 ; Shimizu et al. Cancer Science 2020 ; Shimizu et al. EBioMedicine 2019 他多数あります。
また、「Pythonで実践 生命科学データの機械学習」という書籍を羊土社から上梓しております。日本国内には機械学習の先生もたくさんいらっしゃいますが、その中で最も医療やライフサイエンス実験現場にも精通していると自負しております。
機械の目で正しく見るためには、目的やデータの内容、データの量に応じた対応が必要です。 データの特徴を捉えるための前処理と呼ばれる「下ごしらえ」や、機械学習モデルの種類の選択、パラメータの選択や設定などを適切に行うことで、データの実力を最大限に発揮させることができます。それらを適切に行うためには、機械学習の専門家が持つ経験や、職人技、数学や統計学の知識がとても大切です。そして同じくらい重要なのが、元になるデータの内容や研究分野の専門知識といったドメイン知識です。それらの融合によって、高いレベルの解析が可能になります。


システム生物学・数理モデル構築関連
システム生物学は、数理の言葉で生体内の現象を記述し、そこに潜むルールを見つけシミュレーションを可能にする異分野融合の学問領域です。
ゲノムスケール代謝モデルを用いた解析
ゲノムスケール代謝モデル (genome-scale metabolic model, GEM) とは、細胞内の代謝反応をゲノムワイドに記述したモデルです。フラックスバランス解析など物質収支に基づくシミュレーションを用いて、疾患の理解、薬剤ターゲットの予測、酵素の機能予測、細胞種間の相互作用解析、微生物による有用化合物生産などに利用可能です。ヒト・マウス・微生物を含むGEMを使う環境の整備、トランスクリプトームデータを用いた細胞・組織・個人特有のGEM構築等々、ご興味がございましたらまずはご連絡ください。目的に合わせて適切な方法を用います。必要に応じて新しい手法を考案できる可能性もあります。私達が関わっている解析例としては、Ito et al., bioRxiv 2025他があります。
常微分方程式モデルを用いた解析
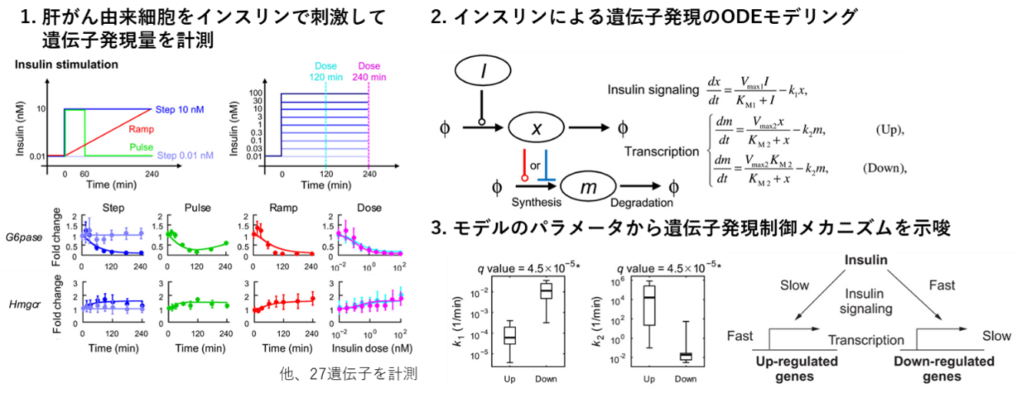
生物学的なメカニズムに基づく常微分方程式 (ODE) モデルの構築、および構築されたモデルの解析です。ODEモデリングに必要な環境の整備、ODEモデルの構築 (対象・データ・計算コスト等を鑑みて総合的に判断)、ODEモデルの解析 (パラメータ感受性解析、安定性解析、信頼区間算出など) 等が実施可能です。私達が関わっている主要ジャーナルに掲載された解析例としては、Hishinuma et al. PLoS Comput. Biol. 2025、Sano et al. Science Signaling 2016 他があります。
同位体トレーサー実験におけるメタボロームデータの解析
炭素の安定同位体13Cを含む化合物のトレーサー実験において、質量分析器によって計測される同位体メタボロームの解析を行います。適切な実験系であれば、生体内や細胞内での代謝経路の活性を解釈できます。可能であれば実験を計画している段階でお声がけください。どのような解釈ができるかは、用いるトレーサーと計測するものに大きく依存します。私達が関わっている主要ジャーナルに掲載された解析例としては、Ohno et al. iScience 2020 ; Krycer et al. Cell Reports 2017 他があります。
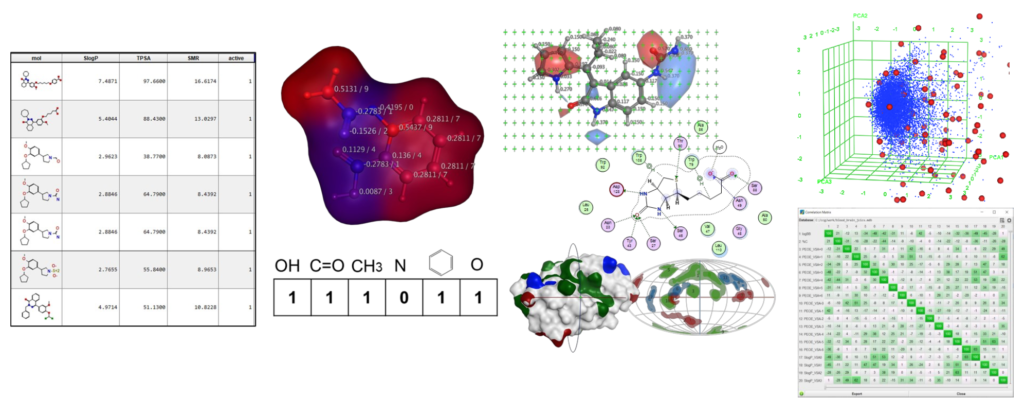
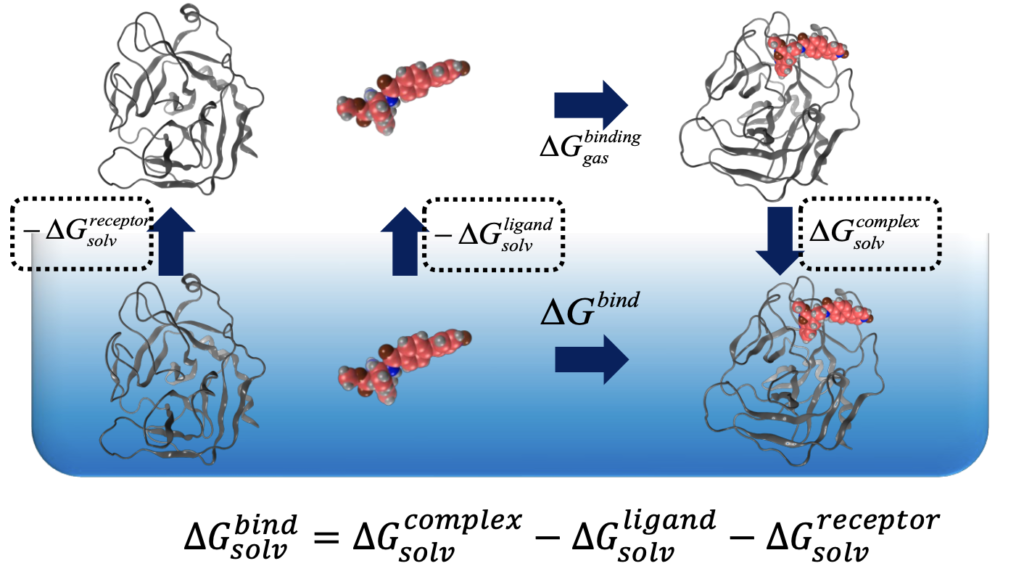
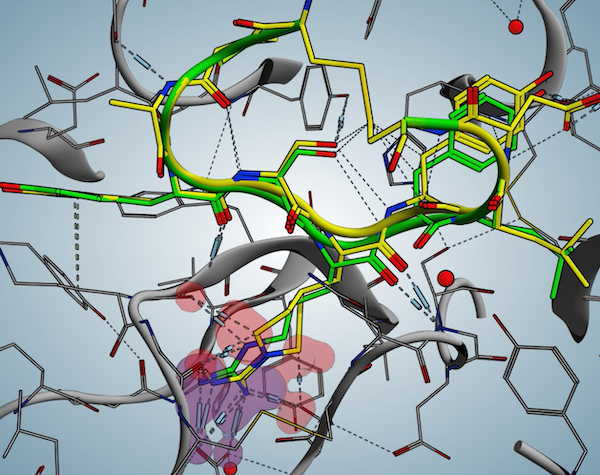
コンピューター創薬関連
その名の通り薬の候補をコンピューターで見つけます。一般的なSBDD (Structure-based drug discovery), LBDD (Ligand-based drug discovery), FBDD (Fragment-based drug discovery) に加え、AI創薬も実施可能です (例えば Shimizu et al. iScience 2022)。中分子創薬は鋭意努力中 (Otani et al., bioRxiv 2025など) ですが、現在のところは共同研究としては低分子のみの探索を行います。私達のところでは製薬会社が持つ創薬のための専用ソフトやクラスター計算環境も常備しておりますので、AI創薬に限らず創薬のさまざまなフェーズにおいて最適な手法をご提案できます。